अध्याय 4 : दहन और ज्वाला (Combustion and Flame)
दहन (Combustion) हमारे दैनिक जीवन में ऊर्जा प्राप्त करने की एक महत्वपूर्ण प्रक्रिया है। जब कोई पदार्थ ऑक्सीजन की उपस्थिति में जलता है और ऊष्मा व प्रकाश उत्पन्न करता है, तो इसे दहन कहा जाता है। यह प्रक्रिया केवल रासायनिक अभिक्रिया नहीं है, बल्कि ऊर्जा परिवर्तन का एक उत्कृष्ट उदाहरण भी है।
दहन के बिना जीवन की कई आवश्यक गतिविधियाँ — जैसे खाना पकाना, वाहन चलाना और बिजली उत्पादन — संभव नहीं हो पातीं।
इस अध्याय में हम दहन के प्रकार, दहन के लिए आवश्यक शर्तें, ज्वाला की संरचना, और विभिन्न ईंधनों की तुलना के बारे में जानेंगे। साथ ही, हम यह भी समझेंगे कि स्वच्छ ईंधन और प्रदूषण नियंत्रण क्यों जरूरी है।
| विषय | संक्षिप्त विवरण |
|---|---|
| दहन क्या है? | ऑक्सीजन की उपस्थिति में किसी पदार्थ का जलना जिससे ऊष्मा व प्रकाश उत्पन्न हो। |
| ज्वाला | दहन के दौरान गैसीय पदार्थों का वह भाग जो प्रकाश देता है। |
| ईंधन | वह पदार्थ जो दहन कर ऊर्जा प्रदान करता है। |
| प्रदूषण | अपूर्ण दहन से उत्पन्न धुआँ और हानिकारक गैसें वायु को प्रदूषित करती हैं। |
मोमबत्ती की ज्वाला में तीन क्षेत्र होते हैं — बाहरी उज्ज्वल भाग, मध्य भाग और भीतरी गहरा भाग। इन सभी क्षेत्रों में तापमान अलग-अलग होता है।
दहन की प्रक्रिया को समझना हमें सुरक्षित ऊर्जा उपयोग, प्रदूषण नियंत्रण और पर्यावरण संरक्षण के प्रति जागरूक बनाता है। इस अध्याय में हम यह भी जानेंगे कि अग्नि शमन (Fire Control) कैसे किया जाता है और किन कारणों से कुछ पदार्थ जलते नहीं हैं।
दहन क्या है? (What is Combustion?)
जब कोई पदार्थ ऑक्सीजन (O2) की उपस्थिति में जलकर ऊष्मा तथा प्रकाश उत्पन्न करता है, तो इस प्रक्रिया को दहन (Combustion) कहा जाता है। यह एक रासायनिक अभिक्रिया है जिसमें ईंधन व वायु की ऑक्सीजन आपस में अभिक्रिया कर ऊर्जा उत्पन्न करते हैं।
“किसी पदार्थ का ऑक्सीजन के साथ रासायनिक अभिक्रिया कर ऊष्मा और प्रकाश उत्पन्न करना, दहन कहलाता है।”
प्रयोग द्वारा दहन को समझें:
एक मोमबत्ती को स्टैंड पर रखें और उसे जलाएं। अब उस पर एक उल्टा काँच का जार रख दें।
कुछ समय बाद आप देखेंगे कि ज्वाला बुझ जाती है।
परिणाम:
ज्वाला बुझने का कारण है कि जार के अंदर की सारी ऑक्सीजन समाप्त हो गई।
निष्कर्ष:
इससे यह सिद्ध होता है कि दहन के लिए ऑक्सीजन आवश्यक है।
| दहन के लिए आवश्यक शर्तें | व्याख्या |
|---|---|
| 1. ज्वलनशील पदार्थ | ऐसा पदार्थ जो जल सके, जैसे लकड़ी, मोम, पेट्रोल आदि। |
| 2. ऑक्सीजन (हवा) | दहन के लिए ऑक्सीजन का होना अनिवार्य है। |
| 3. ताप (Ignition Temperature) | दहन आरंभ करने के लिए पदार्थ को उसकी प्रज्वलन ताप तक गर्म करना पड़ता है। |
यदि इन तीनों में से कोई एक भी शर्त पूरी नहीं होती — तो दहन संभव नहीं होता।
दैनिक जीवन में दहन के उदाहरण:
- मोमबत्ती का जलना
- लकड़ी या कोयले का जलना
- रसोई गैस (LPG) का जलना
- वाहनों में पेट्रोल या डीज़ल का जलना
दहन की यह प्रक्रिया हमारे जीवन के लिए अत्यंत उपयोगी है, परंतु इसके साथ सुरक्षा और प्रदूषण नियंत्रण का ध्यान रखना भी आवश्यक है।
सारणी : दाह्य और अदाह्य पदार्थ
| क्रम सं. | पदार्थ | दाह्यता | वर्गीकरण |
|---|---|---|---|
| 1 | लकड़ी | जलती है और ऊष्मा व प्रकाश देती है | दाह्य पदार्थ |
| 2 | कागज | आसानी से जल जाता है | दाह्य पदार्थ |
| 3 | लोहे की कीलें | नहीं जलतीं, केवल गरम होकर लाल हो सकती हैं | अदाह्य पदार्थ |
| 4 | मिट्टी का तेल | आग के संपर्क में आते ही जल उठता है | दाह्य पदार्थ |
| 5 | पत्थर का टुकड़ा | न तो जलता है और न ही ऊष्मा देता है | अदाह्य पदार्थ |
| 6 | स्ट्रा (घास/फूस) | तेजी से जल जाती है | दाह्य पदार्थ |
| 7 | काष्ठ-कोयला (Charcoal) | धीरे-धीरे जलता है और ऊष्मा उत्पन्न करता है | दाह्य पदार्थ |
| 8 | माचिस की तीलियाँ | घर्षण से जल उठती हैं | दाह्य पदार्थ |
| 9 | काँच | न जलता है, केवल पिघल सकता है | अदाह्य पदार्थ |
1. ज्वलन ताप (Ignition Temperature)
किसी पदार्थ को जलना प्रारंभ करने के लिए जिस न्यूनतम तापमान तक उसे गरम करना आवश्यक होता है, उसे ज्वलन ताप या प्रज्वलन ताप कहा जाता है।
यह तापमान प्रत्येक पदार्थ के लिए अलग-अलग होता है।
कागज का ज्वलन ताप लगभग 233°C होता है जबकि लकड़ी का ज्वलन ताप इससे अधिक होता है।
| पदार्थ | ज्वलन ताप (लगभग) |
|---|---|
| कागज | 233°C |
| लकड़ी | 260°C |
| काष्ठ-कोयला | 400°C |
| केरोसीन | 210°C |
2. आग से बचाव (Fire Safety)
आग से बचाव के लिए सबसे आवश्यक है — दहन की तीन आवश्यक शर्तों (ज्वलनशील पदार्थ, ऑक्सीजन, और ताप) में से किसी एक को समाप्त कर देना।
इसी सिद्धांत पर आग बुझाने के उपाय आधारित हैं।
- बिजली के उपकरणों की आग में पानी का उपयोग न करें।
- गैस या तेल की आग पर रेत या फोम का उपयोग करें।
- घर में फायर एक्सटिंग्विशर रखें।
- ज्वलनशील पदार्थों को खुली आग से दूर रखें।
3. जंगल की आग (Forest Fire)
गर्म और शुष्क मौसम में जंगलों में सूखी पत्तियाँ, लकड़ियाँ और घासें स्वयं जल उठती हैं।
इसे जंगल की आग कहा जाता है।
यह हवा के प्रवाह से तेजी से फैलती है और पर्यावरण को भारी नुकसान पहुँचाती है।
परिणाम: जैव विविधता का ह्रास, मिट्टी की गुणवत्ता में कमी और वायु प्रदूषण।
4. आग बुझाने के यंत्र (Fire Extinguishers)
आग बुझाने के लिए ऐसे उपकरणों का प्रयोग किया जाता है जिनमें गैस, पानी, फोम या सूखे रासायनिक पाउडर (Dry Chemical Powder) होता है।
ये यंत्र दहन की आवश्यक शर्तों को समाप्त कर आग बुझाते हैं।
| आग का प्रकार | उपयुक्त यंत्र / माध्यम |
|---|---|
| कागज, लकड़ी | पानी |
| तेल या पेट्रोल | फोम या CO2 यंत्र |
| बिजली उपकरण | CO2 या Dry Chemical Powder |
| गैस रिसाव | CO2 आधारित यंत्र |
5. ज्वलनशील पदार्थ (Combustible Substances)
वे सभी पदार्थ जो ऑक्सीजन की उपस्थिति में जलकर ऊष्मा तथा प्रकाश उत्पन्न करते हैं, ज्वलनशील पदार्थ कहलाते हैं।
अज्वलनशील पदार्थ: लोहा, काँच, पत्थर, रेत आदि।
हम आग पर नियंत्रण कैसे पाते हैं?
दहन या आग लगने पर ऊष्मा और प्रकाश उत्पन्न होते हैं। लेकिन जब यह अनियंत्रित रूप में फैल जाती है,
तो यह हानिकारक बन जाती है। इसलिए यह समझना आवश्यक है कि हम आग पर नियंत्रण कैसे पा सकते हैं।
आग बुझाने के तीन मुख्य तरीके
- ऑक्सीजन की आपूर्ति रोकना: आग जलने के लिए ऑक्सीजन की आवश्यकता होती है।
यदि ऑक्सीजन की आपूर्ति रोक दी जाए, तो दहन रुक जाता है। उदाहरण के लिए,
जलती मोमबत्ती पर ग्लास रख देने से वह बुझ जाती है। - ईंधन को अलग करना: यदि आग किसी पदार्थ से फैल रही हो, तो उस पदार्थ को हटाकर
या अलग कर देने से आग को रोका जा सकता है। - तापमान कम करना: किसी दहनशील पदार्थ को उसके प्रज्वलन ताप से नीचे ठंडा करने पर
उसका दहन रुक जाता है। उदाहरण के लिए, जल (Water) आग की ऊष्मा को कम करके उसे बुझा देता है।
आग बुझाने के सामान्य उपाय
- जल से आग बुझाना (परंतु विद्युत या तेल की आग पर जल का प्रयोग नहीं करना चाहिए)
- रेत या मिट्टी डालना
- फोम आधारित या कार्बन डाइऑक्साइड (CO₂) आधारित अग्निशामक का प्रयोग
महत्वपूर्ण तथ्य:
विद्युत आग को कार्बन डाइऑक्साइड गैस से बुझाया जाता है क्योंकि यह ऑक्सीजन की परत को हटा देती है
और विद्युत प्रवाह नहीं करती।
निष्कर्ष:
आग पर नियंत्रण पाने के लिए हमें या तो ऑक्सीजन हटानी चाहिए,
तापमान कम करना चाहिए या ईंधन का संपर्क तोड़ देना चाहिए।
इन तीनों तरीकों से किसी भी प्रकार की आग पर प्रभावी नियंत्रण पाया जा सकता है।
दहन के प्रकार
दहन की प्रक्रिया सभी पदार्थों में समान नहीं होती। कुछ पदार्थ तुरंत जलते हैं,
जबकि कुछ बहुत धीरे-धीरे जलते हैं। दहन को इसकी गति और प्रकृति के आधार पर तीन प्रकारों में बाँटा गया है।
दहन के मुख्य प्रकार:
| क्रम सं. | दहन का प्रकार | विवरण | उदाहरण |
|---|---|---|---|
| 1. | तीव्र दहन (Rapid Combustion) | जब कोई पदार्थ ऑक्सीजन के संपर्क में आते ही बहुत तेजी से जलने लगता है और अधिक ऊष्मा व प्रकाश उत्पन्न करता है। | माचिस की तीली जलना, गैस स्टोव की लौ |
| 2. | मंद दहन (Slow Combustion) | जब कोई पदार्थ धीरे-धीरे ऑक्सीजन के साथ प्रतिक्रिया करता है और ऊष्मा उत्पन्न करता है, परंतु प्रकाश नहीं निकलता। | कोयला या लकड़ी का धीरे-धीरे जलना, लोहे का जंग लगना |
| 3. | स्वतः दहन (Spontaneous Combustion) | जब कोई पदार्थ बिना किसी बाहरी ज्वाला या ऊष्मा के स्वयं जल उठता है। | घास या तेल से भरे कपड़े का स्वतः जल उठना |
| 4. | विस्फोटक दहन (Explosive Combustion) | जब बहुत कम समय में अचानक अत्यधिक ऊष्मा, प्रकाश और गैसें उत्पन्न होती हैं। | पटाखों या विस्फोटक पदार्थों का फटना |
Note:-
दहन की प्रकृति पदार्थ के प्रकार और प्रज्वलन ताप पर निर्भर करती है।
तीव्र, मंद, स्वतः और विस्फोटक दहन हमारे दैनिक जीवन में विभिन्न रूपों में देखे जाते हैं।
ज्वाला एवं उसकी संरचना
जब कोई दहनशील पदार्थ जलता है, तो उससे ज्वाला (Flame) उत्पन्न होती है।
ज्वाला वह दृश्यमान प्रकाशमान क्षेत्र होता है जहाँ दहन की प्रक्रिया होती है और ऊष्मा तथा प्रकाश उत्सर्जित होते हैं।
ज्वाला क्या है?
गैसीय दहनशील पदार्थों के जलने पर जो प्रकाशमान भाग बनता है उसे ज्वाला कहा जाता है।
उदाहरण के लिए — मोमबत्ती, गैस स्टोव, और मिट्टी का तेल जलने पर ज्वाला उत्पन्न करते हैं।
ज्वाला के लिए आवश्यक शर्तें
- दहनशील पदार्थ का गैसीय रूप में होना
- ऑक्सीजन की उपस्थिति
- प्रज्वलन ताप प्राप्त होना
ज्वाला की संरचना
ज्वाला के अंदर विभिन्न भाग होते हैं, जिनमें दहन की तीव्रता और तापमान अलग-अलग होता है।
मोमबत्ती की लौ तीन मुख्य भागों में बाँटी जाती है:
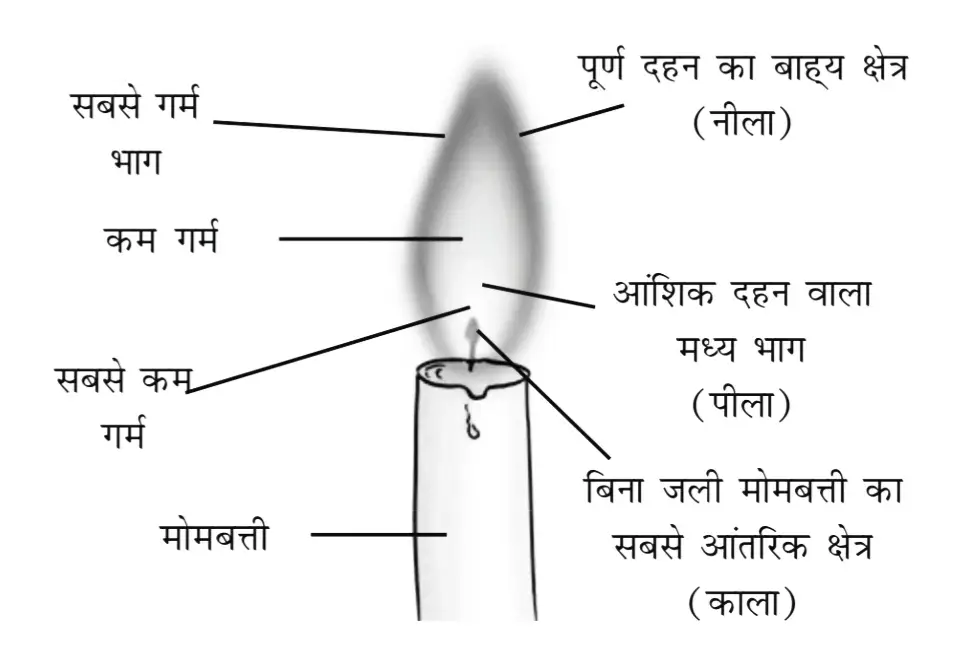
| क्रम सं. | ज्वाला का भाग | विवरण | विशेषताएँ |
|---|---|---|---|
| 1. | भीतरी भाग (Inner Zone) | यह लौ का सबसे अंदरूनी भाग होता है जहाँ मोम का वाष्पीकरण होता है। यहाँ ऑक्सीजन की कमी होती है। | अपूर्ण दहन होता है, तापमान सबसे कम। |
| 2. | मध्य भाग (Middle Zone) | यह लौ का चमकीला पीला भाग होता है जहाँ आंशिक दहन होता है और कालिख (soot) बनती है। | प्रकाश उत्सर्जित करता है, परंतु अपूर्ण दहन। |
| 3. | बाहरी भाग (Outer Zone) | यह लौ का सबसे गर्म और नीला भाग होता है जहाँ पूर्ण दहन होता है। | तापमान सबसे अधिक, पूर्ण दहन, नीली लौ। |
तथ्य:
- ज्वाला का सबसे अधिक तापमान बाहरी भाग में होता है।
- नीली लौ यह दर्शाती है कि दहन पूर्ण हो रहा है।
- पीली लौ में कालिख (Carbon particles) के कारण अधिक प्रकाश निकलता है।
नोट:- ज्वाला की संरचना हमें दहन की प्रक्रिया को समझने में मदद करती है।
इसमें विभिन्न क्षेत्रों में अलग-अलग तापमान और दहन की तीव्रता होती है।
कौन से पदार्थ ज्वाला देते हैं और कौन से नहीं :-
सभी दहनशील पदार्थ जलने पर ज्वाला (Flame) नहीं देते।
केवल वे पदार्थ ज्वाला देते हैं जो दहन के समय गैसीय अवस्था में परिवर्तित हो जाते हैं।
ठोस या धात्विक पदार्थ आमतौर पर बिना ज्वाला के जलते हैं।
सारणी : ज्वाला देने वाले और न देने वाले पदार्थ
| क्रम सं. | पदार्थ | क्या ज्वाला देता है? | विवरण / कारण |
|---|---|---|---|
| 1. | मोम (Wax) | हाँ | मोम गर्म होकर वाष्प में बदल जाती है जो जलकर ज्वाला देती है। |
| 2. | कागज | हाँ | कागज जलने पर गैसीय पदार्थ उत्पन्न करता है और ज्वाला देता है। |
| 3. | लकड़ी | हाँ (आरंभ में) | लकड़ी जलने पर पहले गैसें बनती हैं जो ज्वाला देती हैं, बाद में केवल लाल अंगार रह जाते हैं। |
| 4. | कोयला | नहीं | कोयला ठोस रूप में जलता है, परंतु गैसीय उत्पाद नहीं बनाता, इसलिए ज्वाला नहीं देता। |
| 5. | मिट्टी का तेल (Kerosene) | हाँ | यह तरल रूप में गैसीय अवस्था में जलता है और नीली ज्वाला देता है। |
| 6. | लोहे की कील | नहीं | धातुएँ दहनशील नहीं होतीं, इसलिए ज्वाला उत्पन्न नहीं करतीं। |
| 7. | एल.पी.जी. (LPG) | हाँ | यह गैस रूप में होता है और जलने पर नीली ज्वाला उत्पन्न करता है। |
निष्कर्ष:
केवल वे पदार्थ ज्वाला देते हैं जो जलने पर पहले गैसीय अवस्था में पहुँच जाते हैं।
ठोस या धात्विक पदार्थ जैसे कोयला और लोहा ज्वाला नहीं देते।
ईंधन क्या है ?
वह पदार्थ जो दहन करके ऊष्मा और ऊर्जा उत्पन्न करता है, ईंधन (Fuel) कहलाता है।
ईंधन का उपयोग वाहन चलाने, खाना पकाने, विद्युत उत्पादन तथा औद्योगिक कार्यों में किया जाता है।
ईंधन के प्रकार
| क्रम सं. | ईंधन का प्रकार | उदाहरण |
|---|---|---|
| 1. | ठोस ईंधन (Solid Fuel) | लकड़ी, कोयला, चारकोल, पीट |
| 2. | तरल ईंधन (Liquid Fuel) | पेट्रोल, डीजल, मिट्टी का तेल |
| 3. | गैसीय ईंधन (Gaseous Fuel) | एल.पी.जी., बायोगैस, प्राकृतिक गैस (CNG) |
अच्छे ईंधन के गुण
- अधिक ऊष्मा प्रदान करे।
- सस्ता और आसानी से उपलब्ध हो।
- परिवहन में सुविधाजनक और सुरक्षित हो।
- दहन के बाद हानिकारक धुआँ या अवशेष न छोड़े।
- प्रज्वलन ताप उचित हो।
ईंधन की दक्षता (Fuel Efficiency)
किसी ईंधन द्वारा पूर्ण दहन पर उत्पन्न ऊष्मा की मात्रा को ऊष्मीय मान (Calorific Value) कहा जाता है।
इसे किलो-जूल प्रति किलोग्राम (kJ/kg) में मापा जाता है।
सूत्र:ईंधन दक्षता = उत्पन्न ऊष्मा ÷ प्रयुक्त ईंधन की मात्रा
विभिन्न ईंधनों के ऊष्मीय मान
| क्रम सं. | ईंधन | ऊष्मीय मान (kJ/kg) |
|---|---|---|
| 1. | लकड़ी | 17,000 – 20,000 |
| 2. | कोयला | 25,000 – 33,000 |
| 3. | पेट्रोल | 45,000 |
| 4. | डीजल | 45,000 |
| 5. | एल.पी.जी. (LPG) | 50,000 |
| 6. | बायोगैस | 35,000 – 40,000 |
निष्कर्ष:
ईंधन ऊर्जा का मुख्य स्रोत है।
उच्च ऊष्मीय मान और कम प्रदूषण उत्पन्न करने वाला ईंधन अधिक दक्ष (Efficient Fuel) कहलाता है।
प्रमुख शब्द (Key Terms)
- अम्ल वर्षा (Acid Rain): वायु में उपस्थित हानिकारक गैसों जैसे सल्फर डाइऑक्साइड और नाइट्रोजन ऑक्साइड के जलवाष्प से मिलकर बनने वाली वर्षा।
- ऊष्मीय मान (Calorific Value): किसी ईंधन के जलने पर उत्पन्न होने वाली ऊष्मा की मात्रा।
- दहन (Combustion): किसी पदार्थ का ऑक्सीजन की उपस्थिति में जलना जिससे ऊष्मा और प्रकाश उत्पन्न होते हैं।
- विस्फोट (Explosion): जब गैस या वाष्प अचानक तीव्र गति से फैलती है और ऊर्जा उत्पन्न करती है।
- वनोन्मूलन (Deforestation): वनों का अत्यधिक कटाव या नष्ट होना।
- ज्वाला (Flame): ईंधन के जलने पर उत्पन्न होने वाली उज्ज्वल गर्म गैसों की परत।
- अग्निशामक (Fire Extinguisher): आग बुझाने के लिए प्रयुक्त उपकरण।
- ईंधन (Fuel): वह पदार्थ जो जलकर ऊष्मा प्रदान करता है।
- ईंधन दक्षता (Fuel Efficiency): किसी ईंधन से प्राप्त उपयोगी ऊर्जा की मात्रा।
- विश्व ऊष्णन (Global Warming): पृथ्वी के तापमान में वृद्धि होना।
- आदर्श ईंधन (Ideal Fuel): ऐसा ईंधन जो सस्ता, अधिक ऊष्मा देने वाला, आसानी से उपलब्ध और बिना धुआँ उत्पन्न किए जल सके।
- ज्वलन ताप (Ignition Temperature): वह न्यूनतम तापमान जिस पर कोई पदार्थ जलना शुरू करता है।
- ज्वलनशील पदार्थ (Combustible Substance): वे पदार्थ जो ऑक्सीजन की उपस्थिति में जल सकते हैं।
आपने क्या सीखा
- जो पदार्थ वायु में जलते हैं, दाह्य कहलाते हैं।
- दहन के लिए ऑक्सीजन (वायु में) आवश्यक है।
- दहन के प्रक्रम में ऊष्मा और प्रकाश उत्पन्न होते हैं।
- ज्वलन-ताप वह निम्नतम ताप है जिस पर दाह्य पदार्थ आग पकड़ लेता है।
- ज्वलनशील पदार्थों का ज्वलन ताप बहुत कम होता है।
- आग उत्पन्न करने हेतु आवश्यकताओं में से एक या अधिक को हटा कर आग पर नियंत्रण पाया जा सकता है।
- आग पर नियंत्रण पाने हेतु सामान्यतः जल का प्रयोग किया जाता है।
- विद्युत उपकरणों और तेलों में लगी आग को नियंत्रित करने के लिए जल का उपयोग नहीं किया जाता।
- दहन विभिन्न प्रकार के हैं, जैसे तीव्र दहन, स्वतः दहन, विस्फोट आदि।
- ज्वाला के तीन भिन्न क्षेत्र होते हैं — अदीप्त क्षेत्र, दीप्त क्षेत्र और ज्योतिहीन क्षेत्र।
- आदर्श ईंधन सस्ता, आसानी से उपलब्ध, आसानी से जलने वाला और आसानी से वहन योग्य होता है। इसका ऊष्मीय मान उच्च होता है। यह ऐसी गैसें या अवशेष नहीं छोड़ता जो पर्यावरण को प्रदूषित करते हों।
- ईंधनों की दक्षता और मूल्य परस्पर भिन्न हो सकते हैं।
- ईंधन दक्षता को ऊष्मीय मान द्वारा प्रदर्शित किया जाता है जिसका मात्रक “किलोजूल प्रति किलोग्राम” होता है।
- वायु में बिना जले कार्बन कण खतरनाक प्रदूषक होते हैं और श्वसन कष्ट उत्पन्न करते हैं।
- ईंधन के अपूर्ण दहन से विषैली कार्बन मोनोक्साइड गैस बनती है।
- वायु में कार्बन डाइऑक्साइड की बड़ी हुई मात्रा को विश्व ऊष्णन का कारण बताया जाता है।
- कोयले, डीजल और पेट्रोल के दहन से उत्पन्न सल्फर और नाइट्रोजन के ऑक्साइड अम्ल वर्षा उत्पन्न करते हैं जो फसलों, भवनों और मृदा के लिए हानिकारक होती है।
दहन और ज्वाला — प्रश्नोत्तर
1. दहन की परिस्थितियों की सूची (Conditions required for combustion)
- दहनशील पदार्थ (Fuel): वह पदार्थ जो जल सके — जैसे लकड़ी, कागज, पेट्रोल आदि।
- ऑक्सीजन (Oxidiser): सामान्यतः वायु में उपस्थित ऑक्सीजन; बिना ऑक्सीजन दहन संभव नहीं।
- प्रज्वलन ताप (Ignition temperature): वह न्यूनतम तापमान जिस पर पदार्थ जलना प्रारम्भ कर देता है।
- पर्याप्त रिएक्टेंट व निरन्तर रासायनिक अभिक्रिया: दहन तभी लगातार चलता है जब अभिक्रिया के लिए जरूरी पदार्थ उपलब्ध रहें।
- ईंधन का उपयुक्त भौतिक रूप: कई ठोस पदार्थ ज्वाला तभी देते हैं जब वे पहले गैसीय वाष्प बना लें — इसलिए गैस/वाष्प का होना भी मायने रखता है।
2. रिक्त स्थानों की पूर्ति कीजिए
(क) लकड़ी और कोयला जलने से वायु का होता है — प्रदूषण.
(ख) घरों में काम आने वाला एक द्रव ईंधन है — मिट्टी का तेल (kerosene).
(ग) जलना प्रारम्भ होने से पहले ईंधन को उसके — ज्वलन-ताप (Ignition temperature) — तक गर्म करना आवश्यक है.
(घ) तेल द्वारा उत्पन्न आग को — जल (पानी) — द्वारा नियंत्रित नहीं किया जा सकता.
3. समझाइए कि मोटर वाहनों में CNG के उपयोग से हमारे शहरों का प्रदूषण किस प्रकार कम हुआ है
मोटर वाहनों में पेट्रोल/डीजल के स्थान पर यदि CNG (मुख्यतः मीथेन) का प्रयोग किया जाता है तो निम्न लाभ होते हैं:
- अपूर्ण दहन उत्पाद कम: CNG का दहन अपेक्षाकृत पूर्ण होता है, जिससे कार्बन मोनोऑक्साइड (CO) और हाइड्रोकार्बन (HC) का उत्सर्जन घटता है।
- कण (PM) कम निकलते हैं: डीजल के काले धुएँ (PM2.5/PM10) की मात्रा CNG में कम होती है — इसलिए वायु की गुणवत्ता सुधरती है।
- सल्फर ऑक्साइड कम: CNG में सल्फर की मात्रा नगण्य होती है, अतः SO₂ से जुड़ा प्रदूषण और अम्ल वर्षा का खतरा कम होता है।
- स्थानीय स्वास्थ्य लाभ: स्मॉग, साँस सम्बन्धी समस्याएँ और दृश्यता से जुड़ी परेशानियाँ घटती हैं।
4. ईंधन के रूप में LPG और लकड़ी की तुलना
| पहलू | LPG | लकड़ी |
|---|---|---|
| रूप | गैसीय, सिलेंडर में भरा | ठोस — टुकड़ों/लकडियों के रूप में |
| ऊष्मीय मान | उच्च (कुशल) | कम से मध्यम |
| दहन की शुद्धता | पूर्ण/स्वच्छ दहन — कम धुंआ | अपूर्ण दहन से अधिक धुआँ व राख |
| प्रदूषण | कम — कम पार्टिकुलेट और SOx | अधिक — स्मोक/PM और धुआँ |
| नियंत्रण व उपयोगिता | सरल ऑन/ऑफ नियंत्रण, खाना पकाने के लिए उपयुक्त | नियंत्रण मुश्किल, पारंपरिक उपयोग |
| उपलब्धता व लागत | शहरी क्षेत्रों में उपलब्ध पर लागत अधिक | ग्रामीण/घरेलू में सस्ती व उपलब्ध |
| सुरक्षा | सील वाले सिलेंडर; रिसाव खतरनाक | भंडारण सरल पर आग का जोखिम |
5. कारण बताइए
(क) विद्युत उपकरण से संबद्ध आग पर नियंत्रण पाने हेतु जल का उपयोग क्यों नहीं किया जाता?
पानी विद्युत का चालक है। यदि बिजली से जुड़े उपकरण पर पानी डाला जाए तो:
- वह इलेक्ट्रिक शॉर्ट या करंट फैलाकर लोगों को झटका दे सकता है (electrocution का खतरा)।
- पानी से सर्किट को और नुकसान पहुँच सकता है और आग का खतरा बढ़ सकता है (कुछ परिस्थितियों में)।
इसलिए विद्युत आग के लिए CO₂ या Dry Chemical Powder (non-conductive extinguishers) का प्रयोग किया जाता है।
(ख) LPG लकड़ी से अच्छा घरेलू ईंधन क्यों है?
- ऊष्मीय मान अधिक — कम ईंधन में ज्यादा ऊर्जा।
- दहन साफ़ — कम धुआँ एवं राख, रसोई स्वच्छ रहती है।
- नियंत्रण सरल — नॉब से आग को तुरंत बंद किया जा सकता है।
- स्वास्थ्य प्रभाव कम — फिजिकल स्मोक और पार्टिकुलेट घटते हैं।
(ग) कागज स्वयं सरलता से आग पकड़ता है जबकि एल्यूमिनियम पाइप के चारों ओर लपेटा कागज का टुकड़ा आग नहीं पकड़ता — कारण बताइए
कारण यह है कि एल्यूमिनियम एक अच्छा ताप चालक है। जब कागज एल्यूमिनियम से लिपटा होता है:
- एल्यूमिनियम गर्मी को तेजी से फैलाकर कागज के ताप को कम कर देता है — जिससे वह ज्वलन-ताप तक नहीं पहुँचता।
- यदि लपेटन कस कर हो तो ऑक्सीजन की पहुँच भी कम हो सकती है — ऑक्सीजन न होने पर दहन नहीं होता।
6. मोमबत्ती की ज्वाला का चिन्हित चित्र
Outer Zone (बाहरी भाग)
– पूर्ण दहन
– उच्च ताप, नीली लौMiddle Zone (मध्य भाग)
– आंशिक दहन
– पीली ज्वाला, कालिख बनती है
Inner Zone (भीतरी भाग)
– वाष्पीकरण का क्षेत्र, ऑक्सीजन कम
– अपूर्ण दहन
7. ईंधन के ऊष्मीय मान को किस मात्रक द्वारा प्रदर्शित किया जाता है?
ईंधन के ऊष्मीय मान (Calorific value) को सामान्यतः किलो-जूल प्रति किलोग्राम (kJ/kg) में प्रदर्शित किया जाता है।
पारंपरिक रूप से कभी-कभी किलोकैलोरी प्रति किलोग्राम (kcal/kg) भी उपयोग होता है, पर SI इकाई kJ/kg अधिक मान्यता प्राप्त है।
8. समझाइए कि CO₂ किस प्रकार आग को नियंत्रित करती है।
CO₂ (कार्बन-डाइऑक्साइड) आग बुझाने में निम्न तरीकों से सहायक होती है:
- ऑक्सीजन को विस्थापित करना (Smothering): CO₂ गैसीय रूप में भारी होती है और आग के आस-पास मौजूद ऑक्सीजन को हटाकर या dilute करके दहन-प्रतिक्रिया के लिए उपलब्ध ऑक्सीजन की सांद्रता कम कर देती है। जब आवश्यक ऑक्सीजन नहीं बचती, तो दहन रुक जाता है।
- ताप को कम करना (Cooling — कुछ हद तक): CO₂ स्वयं बहुत शक्तिशाली कूलिंग एजेंट नहीं है पर CO₂ को द्रव रूप में परिवर्तन या उच्च-दाब से छोड़ने पर उस स्थान की तापमान में थोड़ी गिरावट आती है, जिससे आग की तीव्रता कम होती है।
- अग्निशामक के रूप में उपयुक्तता: CO₂ गैर-चालक गैस है, इसलिए विद्युत उपकरणों पर उपयोग के लिए सुरक्षित है (पानी के विपरीत)। वही कारण CO₂ extinguisher को इलेक्ट्रिकल fire और तरल-ईंधन आग के कुछ प्रकारों में उपयोगी बनाता है।
9. हरी पत्तियों के ढेर को जलाना कठिन होता है परन्तु सूखी पत्तियों में आग आसानी से लग जाती है — समझाइए।
इसके मुख्य कारण:
- नमी (Moisture) की उपस्थिति: हरी पत्तियाँ अधिक मात्रा में पानी/नमी रखती हैं। आग लगाने पर पहले पानी को वाष्पित करने के लिए ऊष्मा खर्च होती है — इसलिए ऊर्जा का एक बड़ा भाग नमी को उड़ाने में चला जाता है और पत्तियों का ताप जल्दी ज्वलन-ताप तक नहीं पहुँचता।
- ऊष्मीय इनर्शिया: पानी की वाष्पीकरण में ऊष्मा अवशोषित होती है (latent heat of vaporisation), इसलिए नमी वाली सामग्री का ताप वृद्धि धीमी होती है।
- रासायनिक अवस्था: सूखी पत्तियाँ लो-नमी वाली होने से जल्दी गैसीय वाष्प बनाती हैं और उनका ज्वलन-ताप जल्दी पहुँच जाता है, अतः वे आसानी से ज्वलित हो जाती हैं।
- ढेर की घनता व वायु प्रवाह: हरे पत्तों में कुछ स्थानों पर वायु का प्रवाह कम और सूप्त होता है; परन्तु मुख्य कारण नमी ही है।
10. सोने और चाँदी को पिघलाने के लिए स्वर्णकार ज्वाला के किस क्षेत्र का उपयोग करते हैं और क्यों?
स्वर्णकार (goldsmiths) तथा धातु कारीगर ज्वाला का बाहरी नीला भाग (Outer zone) उपयोग करते हैं क्योंकि:
- बाहरी भाग में दहन पूर्ण होता है और तापमान सर्वाधिक होता है।
- उच्च ताप की वजह से धातुओं को जल्दी और समान रूप से पिघलाया जा सकता है।
- नीली लौ कम स्याही/कालिख उत्पन्न करती है और अधिक शुद्ध हीटिंग देती है, जिससे धातु की सतह पर हानिकारक अवशेष कम बनते हैं।
11. (गणितीय प्रश्न) — एक प्रयोग में 4.5 kg ईंधन का पूर्णतया दहन किया गया। उत्पन्न ऊष्मा का माप 180,000 kJ था। ईंधन का ऊष्मीय मान परिकलित कीजिए।
ऊष्मीय मान = (उत्पन्न ऊष्मा) ÷ (ईंधन की मात्रा)
दिए गए: उत्पन्न ऊष्मा = 180,000 kJ ; ईंधन द्रव्यमान = 4.5 kg
गणना (कदम-दर-कदम):
- हम विभाजन 180,000 ÷ 4.5 करें।
- दशमलव विभाजन से बचने हेतु, गुणा करें दोनों पक्षों को 10 से:
180,000 × 10 = 1,800,000 ; 4.5 × 10 = 45.
अतः समतुल्य भाग: 1,800,000 ÷ 45 - अब 1,800,000 ÷ 45 करें — सरल तरीका: पहले 1,800,000 ÷ 5 फिर ÷ 9 क्योंकि 45 = 5 × 9.
1,800,000 ÷ 5 = 360,000.
अब 360,000 ÷ 9 = 40,000. - अतः ऊष्मीय मान = 40,000 kJ/kg.
उत्तर: ईंधन का ऊष्मीय मान = 40,000 kJ/kg.
12. क्या जंग लगने के प्रक्रम को दहन कहा जा सकता है? विवेचना कीजिए।
जंग लगना (rusting) और दहन दोनों में ही ऑक्सीजन की भागीदारी होती है पर वे एक समान प्रक्रिया नहीं हैं। प्रमुख अंतर:
- प्रकिया की तीव्रता: दहन एक तीव्र/ऊर्जा-उत्सर्जक रासायनिक अभिक्रिया है जिसमे ऊष्मा और अक्सर प्रकाश निकलते हैं। जंग लगना धीमी ऑक्सीकरण प्रक्रिया है जो धीरे-धीरे होती है और सामान्यतः ऊष्मा/प्रकाश का स्पष्ट उत्सर्जन नहीं होता।
- उत्पाद और लक्षण: दहन में जलन, लौ और ऊष्मा दिखाई देती है; जंग में लोहे का ऑक्साइड बनता है (रंजक-रंग: भूरे/लाल-भूरे), पर कोई लौ नहीं होती।
- आवश्यकता और अवस्था: जंग अक्सर नम (आर्द्र) परिस्थिति में जल-आवश्यकता के साथ तेज होती है (इलेक्ट्रोकैमिकल प्रक्रियाएँ), जबकि दहन के लिए प्रायः उच्च ताप (प्रज्वलन ताप) की आवश्यकता होती है।
- निष्कर्ष: भौतिक दृष्टि से जंग को ऑक्सीकरण की एक धीमी प्रकार कहा जा सकता है, पर वैज्ञानिक एवं व्यवहारिक रूप से जंग को दहन (combustion) नहीं कहा जाता। कारण — जंग में लौ, तीव्र ताप या प्रकाश का अभाव और प्रक्रिया की धीमी प्रकृति।
13. आबिदा और रमेश के प्रयोग में — किसका पानी कम समय में गर्म होगा?
आबिदा ने बर्तन (बीकर) को मोमबत्ती ज्वाला के पीले भाग (मध्य/दीप्त भाग) के पास रखा; रमेश ने बर्तन को ज्वाला के सबसे बाहरी भाग (नीला भाग) के पास रखा।
उत्तर: रमेश का पानी कम समय में गर्म होगा।
कारण:
- ज्वाला का बाहरी नीला भाग सबसे अधिक तापमान वाला क्षेत्र होता है (पूर्ण दहन होता है)।
- बाहरी क्षेत्र में ऊष्मा का कन्सन्ट्रेशन और ऊर्जा का प्रवाह अधिक होता है, अतः वह किसी आस-पास रखे बर्तन को जल्दी गर्म कर देगा।
- पीला मध्य भाग अपेक्षाकृत ठंडी और आंशिक दहन वाला होता है; वहाँ ऊर्जा का उपयोग मुख्यतः प्रकाश देने में और कालिख उत्पादन में जाता है।
External References for Chapter: दहन और ज्वाला
- NCERT Class 8 Science Chapter 6: Combustion and Flame (Official PDF) – NCERT की आधिकारिक ई-पुस्तक जिसमें पूरा अध्याय हिंदी और अंग्रेज़ी दोनों में उपलब्ध है।
- CBSE Curriculum 2024–25 (Science Syllabus) – CBSE के नवीनतम पाठ्यक्रम में “Combustion and Flame” अध्याय की स्थिति जानें।
- BYJU’S NCERT Solutions for Class 8 Science Chapter 6 – प्रश्नोत्तर सहित विस्तृत व्याख्या।
- Tiwari Academy – Class 8 Science Chapter 6 in Hindi – आसान भाषा में समझाया गया पूरा अध्याय और हल।
- TopperLearning – Combustion and Flame Summary & Solutions – संक्षेप और इंटरएक्टिव प्रश्नोत्तर अभ्यास।
Internal Links – Related Science Notes on InspireVeda
- Class 6 Science – NCERT Notes and Solutions : कक्षा 6 विज्ञान के सभी अध्यायों के नोट्स, प्रश्नोत्तर और अभ्यास प्रश्न।
- Class 7 Science – NCERT Notes in Hindi : सभी अध्यायों का सरल हिंदी में सारांश और समाधान।
- Class 8 Science – NCERT Notes in Hindi : “दहन और ज्वाला” सहित सभी अध्यायों के संपूर्ण नोट्स और अभ्यास प्रश्न।
- Class 9 Science – NCERT Notes in Hindi : विस्तृत व्याख्या और परीक्षा आधारित प्रश्नोत्तर।
- Class 10 Science – NCERT Notes in Hindi : भौतिकी, रसायन और जीवविज्ञान के सभी महत्वपूर्ण अध्याय।
- Class 10 Samkalin Bharat – History Notes (UP Board) : इतिहास के अध्यायों के विस्तृत हिंदी नोट्स।
- Class 11 Biology – Notes in Hindi & English : NEET और बोर्ड परीक्षा हेतु महत्वपूर्ण बायोलॉजी नोट्स।
